亜塩素酸水の主たる有効成分であるクロラス酸による
新型コロナウイルスの不活化が確認できました
新型コロナウイルス(SARS-CoV-2)不活化(除去)効果確認試験報告書(1)
試験条件
| 試験検体 | 亜塩素酸水製剤 含量(亜塩素酸 HClO2 = 68.46)として0.8%[製造時] 遊離塩素濃度(Cl=35.45として)200mg/L 以上 |
|---|---|
| ウイルス株 | SARS-CoV-2(2019-nCoV/Japan/AI/I-004/2020)株 (国立感染症研究所より分与) |
| 宿主細胞 | VeroE6/TMPRSS2 細胞(JCRB1819) |
| ウイルス液中 FBS 濃度 | 0% |
| ウイルス培養時の培地 | Dulbecco's Modified Eagle Medium(DMEM) (富士フィルム和光純薬) |
| ウイルス力価検出法 | TCID50法 |
| ウイルス液:サンプル液反応液比率 | 1:9 |
| 初発ウイルス濃度 | 約 2×10⁷ TCID50 /mL |
検体の調整
試験検体:亜塩素酸水製剤をポリスチレンチューブを用いて蒸留水で希釈した。 尚、ウイルスとの反応もポリスチレンチューブ内で行った。又、このウイルス液と試験検体:亜塩素酸水製剤の希釈液は(1:9)の比で混合し、反応させた。
ウイルス液の調製
VeroE6/TMPRSS2 細胞(10-cm ディッシュ)に m.o.i.が約 0.01 になるようにウイルス液を細胞に接種させ、1 時間後に接種液を吸引除去して血清非含有 DMEM(5 ml)を入れて培養した。細胞変性効果が細胞全体に広がって細胞がはがれ始めたところで培養上清を回収し、低速遠心と 5-µm フィルターで細胞を完全に除いてウイルス液とした。
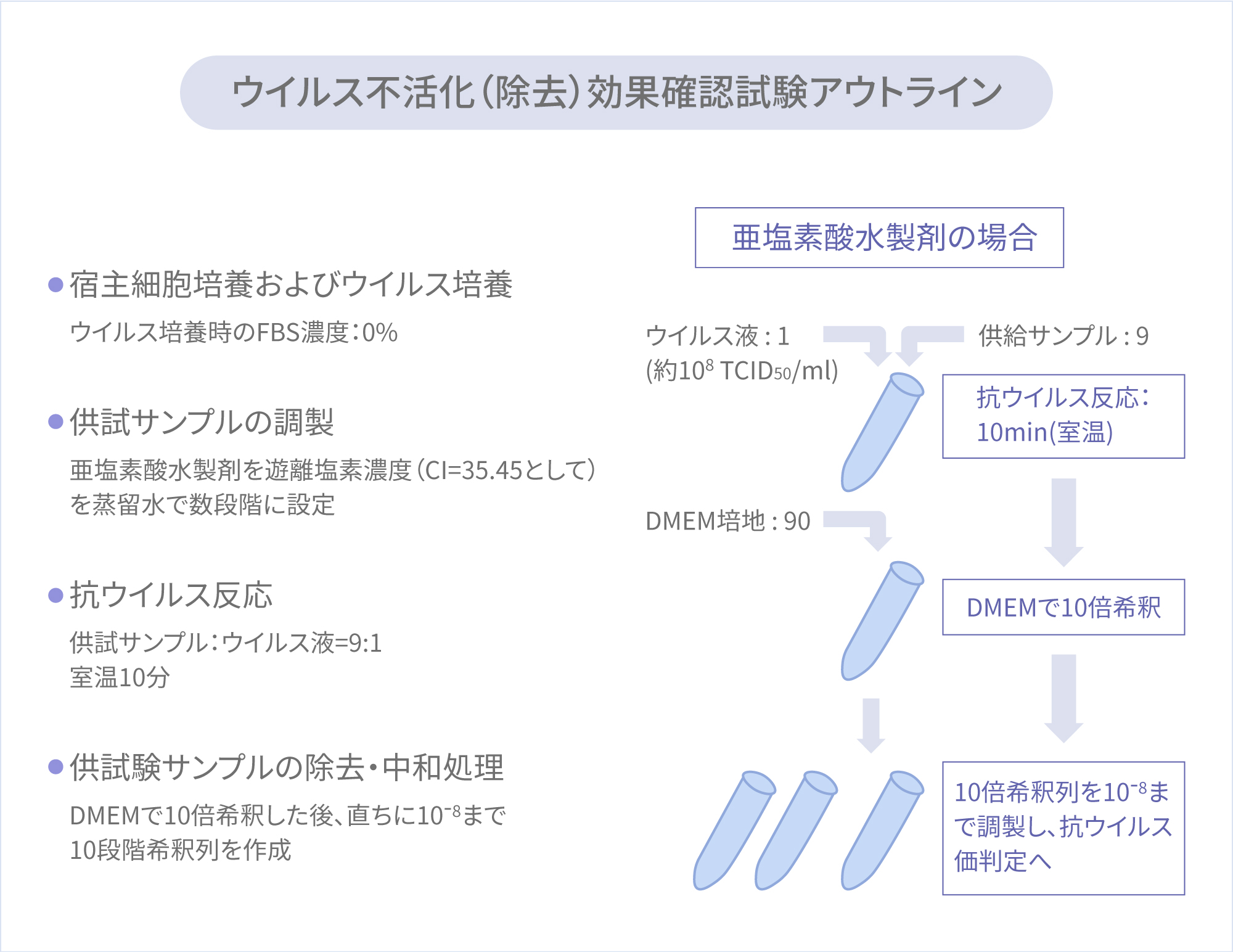
ウイルス不活化(除去)効果確認試験の方法
ウイルス液と試薬を(1:9)の比率で混合し、室温で所定の時間反応させたのちに血清非含有DMEM で 10 倍に希釈して反応を止めた。さらに 10-8 まで 10 倍段階希釈をおこなった。次にVeroE6/TMPRSS2 細胞(96 ウェルプレート)の 4 個のウェルに各希釈のウイルス液を 50µl/well で接種させ、一時間後に吸引除去して 100µl/well の血清非含有DMEM に置換して培養した。3 日後に各ウェルの感染の有無を判定して、Behrens-Karber 法で 50%感染希釈を計算し、ウイルス感染価[50% Tissue culture infectious dose (TClD50)/ml]を求めた。
結果
[ウイルス不活化(除去)効果確認試験]
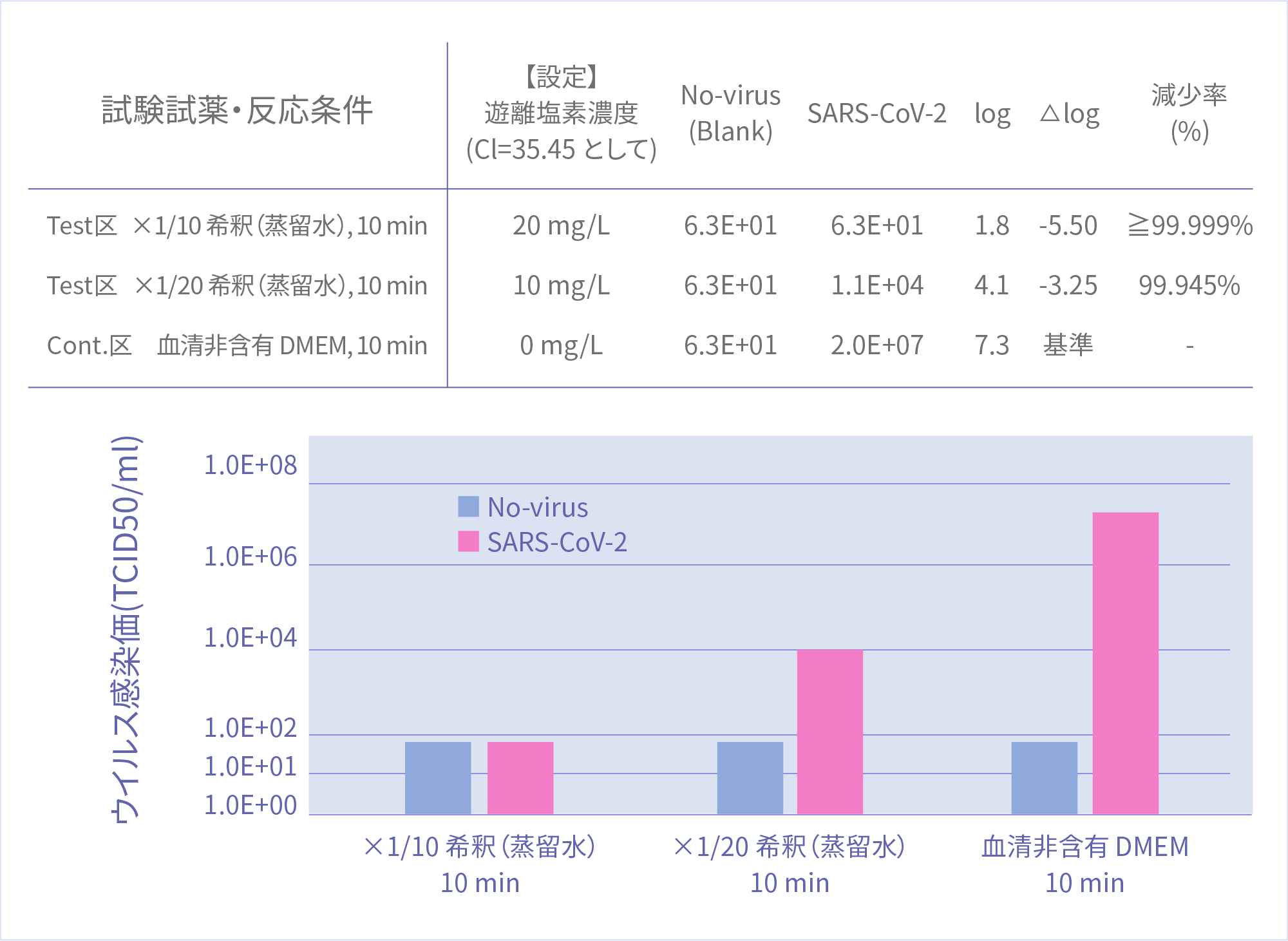
試験検体:亜塩素酸水製剤 1/10 希釈液(遊離塩素濃度(Cl=35.45 として)20mg/L)でウイルス感染価は検出限界(6.3×10) 以下にまで低下[5.5Log 以上(≧99.999%)が除去]していた。なお、この感染価は検出限界であり、ウイルス感染細胞は全く観察されていない。よって、実際の感染価はこれよりも低く、このウイルスは完全に除去(不活化)されたと考えることができる。また、試験検体:亜塩素酸水製剤 1/20 希釈(遊離塩素濃度(Cl=35.45 として)10 mg/L)でも未処理(血清非含有 DMEM)に比べると、ウイルス感染価を1/1000 以下にまで低下[3.25Log (99.945%)が除去]しており、SARS-CoV-2 に対する除去(不活化)効果※はあるといえる。
※効果の評価は、平成 27 年度 ノロウイルス不活化条件に関する調査報告書(国立医薬品食品衛生研究所)の評価基準に準じている。
尚、本試験の結果は、広島大学大学院医系科学研究科ウイルス学 坂口 剛正教授が実施された試験結果の報告書(未発表)に基づき三慶グループが作成したものを引用し、 レック株式会社が作成したものである。
登録日:

